製氧(yǎng)機呼吸機出口(kǒu)印度須知(歸類、資(zī)質、準入條(tiáo)件)
來源: 更新:2021-05-19 19:09:33 作者: 瀏覽:2495次
近期,新冠肺炎疫情在印度(dù)蔓延。呼吸機、製氧機作為抗擊疫(yì)情重要的物(wù)資在印度需求量較大。我們緊急整理(lǐ)匯總出口(kǒu)須知,向相關企業介紹如何順利、有序向印度出口醫療器械。
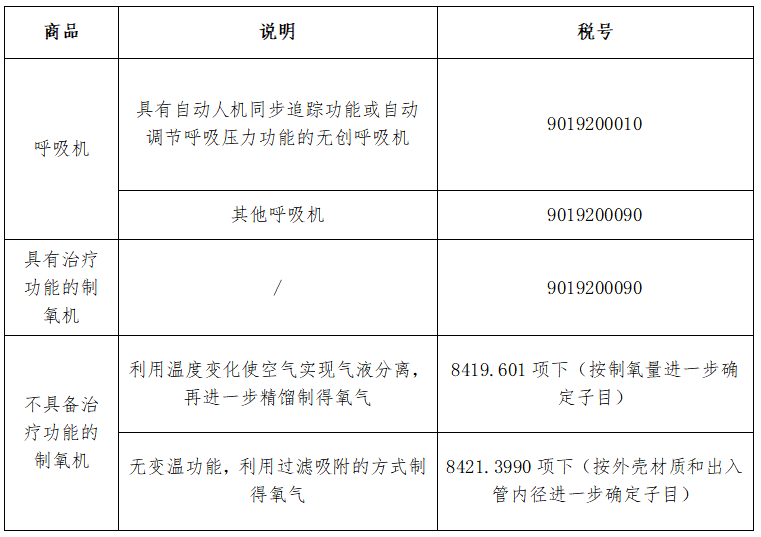
商(shāng)品歸類(根據2021年進出口稅(shuì)則)
呼吸機出口時(shí)需具備的資(zī)質及(jí)材料
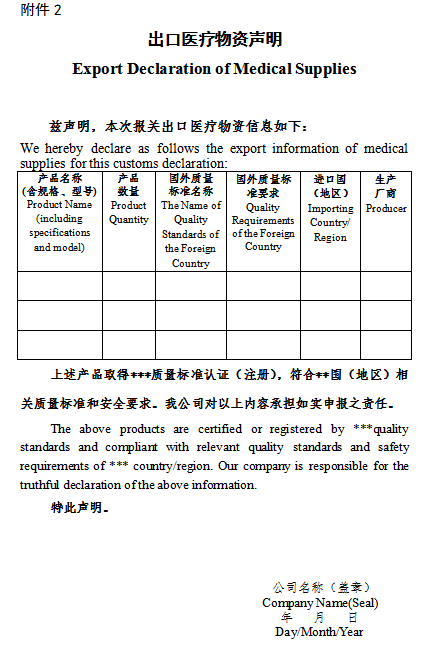
第一種情(qíng)況:產品已取(qǔ)得我國醫療(liáo)器械產品注冊證書,符合進口國(地(dì)區)的質量標準(zhǔn)要求根據(jù)《關於有序開展醫療物資(zī)出口的公告》(商務部 海關(guān)總署 國家藥品監(jiān)督管理(lǐ)局公告2020年第5號)規定,出口呼吸機的企業向海關報關時(shí),須提供書麵或電子聲明,承諾出口產品已取得我國醫療器(qì)械產品注冊(cè)證書,符合進口國(地(dì)區)的質量標準要求,海關憑藥品監督管理(lǐ)部門批準的醫療器械產品注冊(cè)證(zhèng)書(shū)驗放。第二種情況:產品取得國外標準(zhǔn)認(rèn)證或注冊根據《關於進一(yī)步加強防疫物資出口質量監管的(de)公告》(商務部 海關總署(shǔ) 國家市場監督管理總局公告2020年第12號)規定,產品取得國外標準認證或(huò)注(zhù)冊的呼吸機出口企業,報關時須提交(jiāo)電子或書麵聲明,承諾產品符(fú)合進口(kǒu)國(地區)質量標準(zhǔn)和安全要求,海關憑商務(wù)部提供的國(guó)外標準認證或注冊的生產企業清單驗放。第三(sān)種情況:產品不屬於上述公告範(fàn)圍不屬於上述公告範圍內的呼吸機配件、製(zhì)氧機等商品,不用按公告要求(qiú)提供相關單(dān)證。但屬於醫療器械的,應遵守《醫(yī)療(liáo)器械(xiè)監督管(guǎn)理條(tiáo)例》(國務院令680號)要求,即:出口醫療器械的(de)企業應當(dāng)保證其出口的醫療器械符合(hé)進(jìn)口國(guó)(地區)的要求。
本文歸類列(liè)表(biǎo)所列商品出(chū)口退(tuì)稅稅率均為13%。印度衛生和家庭福利部(Ministry of Health & FW)下的中央藥品標(biāo)準控製局(Central Drug Standards Control Organization,簡稱CDSCO)為印度醫療器械的(de)中央主管機構,其內部的(de)重要組成機構印度藥品(pǐn)管理總局(The Drug Controller General of India,簡稱DCGI)作(zuò)為印(yìn)度全國醫療器械政策的製定單位。2017年印(yìn)度對醫療器(qì)械法規進行(háng)了大(dà)幅修訂,公布了《醫療器械管理條例2017》(Medical Device Rules 2017),從2018年1月起實施,參照了“全球醫療器械法規(guī)調和會”(The Global Harmonization Task Force,簡稱GHTF),將醫(yī)療器械分為A到D四類(lèi),對應從(cóng)低風險到高風險四種風險級別。印度CDSCO在2017年也(yě)發布了《醫療器械與體外診療醫(yī)療(liáo)器械分類標準》,印度要求在申請產品登記時,應遵循印度藥品管理總局(DCGI)針對醫療(liáo)器械的分類決定。對於未能判斷分類的(de)情況(kuàng),應向CDSCO提出分類申請。
出口印度醫療(liáo)器械(xiè)製造許可證的申請
出(chū)口醫療器械至印度進行銷售或使用,必須經印度當地授權代理人(authorised agent)向CDSCO提(tí)出醫療器(qì)械進口許可證申請(包括A至D級)。CDSCO對醫療器械進口許可(kě)證(zhèng)的審核(hé)主要分為兩步:第一步:確認生產企業質量管理體係(Quality Management System,簡稱QMS)的符合性首先CDSCO審核授權代理人所提交的生產企業質量管理體係,其必須符合印度醫療器械質量管理標準ICMED 13485(修改采用自ISO 13485,我國標準YY/T 0287等(děng)效采用了ISO 13485),包括:生產企業QMS技術文件、檢測報告、最近一次現場檢查報告等,如果CDSCO認定生產企(qǐ)業QMS的符合存在疑(yí)慮(lǜ)時,可以要求實施評估、產品檢測(cè)或生產企業現場檢查(費用由代理人承擔)。第二步(bù):審(shěn)核醫療器械的安全性與有效性如果出(chū)口印度的醫療器械分類屬於A級或(huò)者B級,授權代理人應向CDSCO提交中國的自由銷售證明,或者(zhě)中國實施臨床測試的數據(或其他可供證明產品安全性與有效性的數據)。如(rú)果出口(kǒu)印度的醫(yī)療器械分類屬(shǔ)於C級或者D級,授權代理人必須在(zài)印度實施臨床測試(shì)。例(lì)外情況(kuàng):如果醫療器械(A級至D級)已由歐盟、美國、加拿大、日本或澳大利亞的監管機構頒發了自由銷售(shòu)證明,則無需再進行臨床測試。印度《醫療器械管理條例2017》第44條至48條(tiáo)對醫療器械的標簽進(jìn)行了要求。醫療器(qì)械標簽要求:該條例第44條規定,應用不可抹掉的墨水在醫療器械的(de)架子包裝上或醫療器械的外殼上以及在(zài)包裝醫療器(qì)械的每個外殼上印刷以下內容:03.製造商的名稱和(hé)製造(zào)該設(shè)備的製造場(chǎng)所的地址。04.關於淨數量的正確說明,應以重量、尺寸、體積、單位數量(視情況而定)以及包裝中所含設備的數(shù)量以公製表(biǎo)示(shì)。05.生產年月及有效期(qī)(或者標簽應標明產品的保質期)。06.在需要時提供指示,以表明該器械含(hán)有藥用(yòng)或生物物質。07.提供一個明顯的批號(hào),並以“Lot No.”一(yī)詞開頭(tóu)或“Lot”或“Batch No.”或“B. No.”。08.在需要時指出適用於該(gāi)設備的(de)任何特殊存儲或(huò)處理條件。09.指明該裝(zhuāng)置是否以無菌產品形式提供,及其無菌狀態和滅菌方法。10.給予警告或預防措施(如果認為相關的話),以引起醫療器械使用者的注意。11.如果該設備是一次性使用的,則應適當標記該設備。12.如果打(dǎ)算將醫療器械作為(wéi)免費樣品分發給醫療專業人(rén)員,則在該器(qì)械的標簽上套(tào)印“Physician’s Sample—Not to be sold”字樣。13.除進口設備外,在“Manufacturing Licence Number”或“Mfg. Lic. No.” 或“M. L”之前加上製造(zào)許可證號。14.如果是進(jìn)口設備,則在標簽上通過粘貼方式提供(如果尚未打印)此類細節,包(bāo)括:進口(kǒu)許可證編號、進口商的名稱(chēng)和地址、實際生產場所的地址以及製造日期。15.如果小型醫療器械因為體積原因,無法清晰打印所有信息,則至少應包括產品識(shí)別和安(ān)全所需的信息。例如:第1、2、3、4條(tiáo)款所涵蓋的信息,第5、7、11和13應包括在內。唯一的器械標識:條例第46條規定,自2022年1月1日(rì)起,經(jīng)批準製造、銷售、分銷或進(jìn)口(kǒu)的醫療器械(xiè)應帶有唯一的器械標識,其中應包含器械標識符和生產標識符(fú)。其中:02.“生產標識符”是指序列號、批次或批號、醫療器械軟件版本號、製造(zào)日期和或有效期。
印度財政部已於2021年4月24日發布第28/2021-Customs公(gōng)告,取消製氧機(HS 9019/HS 842139) 、呼吸機(HS 9019)等18項產品進口關稅,至2021年7月31日止。印度港口、航運暨(jì)水道部也(yě)於25日通知各主要港口,取消進口氧氣及相關設備的港口處理費(fèi),給予優先泊船通關。港務人員必須嚴格控製船舶(bó)入(rù)港及貨物(wù)通關時(shí)間,協(xié)助物流運作。








![]() 京公網安備(bèi) 11011302005837號
京公網安備(bèi) 11011302005837號